|
《细胞和分子免疫学》 > 第十章 神经免疫内分泌学引论
第三节 神经和内分泌(或神经内分泌)系统对免疫系统的调控神经免疫内分泌学中一重要方面是神经和内分泌系统(或神经内分泌)对免疫功能的调控。广义上讲,所有的内分泌功能均受神经系统的直接或间接支配,故神经和内分泌系统可以神经内分泌表示。神经内分泌对免疫系统的影响是由激素、神经肽、神经递质的作用所实现,体现于一些典型的生理过程或实验过程中,如应激、妊娠、哺乳或条件性免疫应答的产生等。
一、神经内分泌对免疫功能调控的生物学基础(一)免疫组织及器官上的神经支配淋巴组织和淋巴器官具有神经去配是久已周知的事实,这些神经纤维伴随血管穿过被膜而进入淋巴组织,其性质为交感或副交感神经纤维。近年大量工作表明,支配中枢和外周淋巴器官的神经含有众多肽能神经纤维。 1.髓髓 脊神经中的内脏纤维伴骨动脉经滋养孔进入骨髓,支配骨髓内血管及实质,与细胞关系密切。这些纤维包括有髓和无髓纤维,其中有P物质(substance P,SP)肽能神经纤维。 2.胸腺 作为中枢免疫器官和内分泌器官,胸腺可接受膈神经、交感神经和副交感神经支配,其中交感神经纤维来源于颈胸段交感神经链,而副交感纤维来源于迷走神经。用免疫组织化学逆行追踪法证实,支配胸腺的迷走神经纤维发自延髓的面后核、颖核、迷走神经背核等核团,并接受网状系统的传入冲动,与高级中枢间构成多突触联系。这些迷走神经节前神经元含有高脑啡肽(leucine-enkephalin,L-ENK)和生长抑素(SS)。在发育早期,迷走神经纤维即分布于胸腺,进而形成神经网。这些神经纤维随腺体的发育、成熟和衰退而变化。交感和副交感神经纤维在皮质中成丛分布,游离末梢进入髓质,与各种细胞相比邻。血管活性肠肽(vasoactive intestinal polypeptide,VIP)、降钙素基因相关肽(calcitonin-gene-related polypeptide,CGRP)及神经肽Y(neuropeptide Y,NPY)阳性的神经分布于大鼠胸腺血管周围,小叶间结缔组织及皮质和髓质的实质内。被膜中有SP及CGRP阳性纤维和去甲肾上腺素(norepinephrine,NE)能神经纤维分布,并有分支穿插于胸腺实质细胞间,与肥大细胞及巨噬细胞关系密切。已发现NPY亦共存于NE能神经末梢中。这些事实说明胸腺的结构和机能可受交感和副交感神经活动的影响。一般认为交感神经兴奋可减弱免疫机能,而副交感神经兴奋则作用相反。 3.脾 来自腹腔神经节的交感神经形成脾神经沿脾门入脾,迷走神经伴动脉入脾,进入脾实质白髓的小动脉树,与淋巴细胞关系密切,尤其在白髓和红髓的交界处。大鼠脾脏白髓中央动脉及其分支上有NPY,甲硫氨酸脑啡肽(methionine-enkephalin,M-ENK)缩胆囊素(cholecystokinin,CCK)和神经降压素(neurotensin,NT)阳性神经纤维分布,仅少数进入实质。猫脾脏血管中亦含有NPY、SP及VIP免疫阳性神经纤维。已发现NPY与NE共存。这种纤维主要见于脾脏被膜和小梁部位的血管。另外酪氨酸羟化酶(tyrosine hydroxylase,TH)阳性神经末梢可与脾淋巴细胞形成突触联系。 4.淋巴结 在淋巴结的包膜下及包膜内,可见乙酰胆硷(acetylcholine,ACh)能神经纤维,而NE能神经进入淋巴结实质中,绕周边血管成丛分布,少许在实质中游离。在淋巴结的门部、被膜下、皮质与髓质交界及髓质和副皮质区有SP、VIP、NPY、CGRP等肽能神经纤维的分布。 5.淋巴管 交感和副交感神经纤维支配淋巴管,并有区域性特点。另外,肠壁粘膜下层的淋巴小结或Peyer氏结与粘膜免疫密切相关,并受SP肽能神经纤维的支配。SP肽能神经纤维还存在于肠绒毛中央乳糜管周围,后者还有ACh能神经纤维分布。 以下上事实说明,免疫组织和器官受到交感神经、副交感神经和肽能神经纤维的支配,从形态上体现出神经系统对免疫系统的直接影响,这种神经支配可以突触方式和非典型突触两种方式,即“线性传导”和“体积性传导”,后者应视为神经纤维末梢的旁分泌现象。至于整体条件下两种方式何者为主,尚不知晓。神经纤维对淋巴组织和器官的影响至少涉及以下几方面:①血流调控;②淋巴细胞的分化、发育、成熟、移行和再循环;③细胞因子或其它免疫因子的生成和分泌;④免疫应答的强弱及维持的时间等。 (二)免疫细胞上的受体分布运用药理学方法、放射受体分析、放射自显影、受体生化和受体分子生物学等技术,已在免疫细胞膜上或胞内发现众多激素、神经肽和神经递质的特异性受体。 1.经典神经递质受体 (1)肾上腺素受体:肾上腺素能受体可分为α和β两型,并可再分为α1、α2和β1及β2型。已知胸腺和脾接受肾上腺素能纤维的支配,并发现在胸腺细胞和脾细胞膜上有β受体的分布。小鼠胸腺细胞β受体在胚胎期的亲和力(Kd=2.2nM)高于成年鼠(Kd=8.0nM)。用β受体激动剂异丙肾上腺素刺激后,胎鼠胸腺细胞cAMP增高也更为明显。小鼠淋巴细胞上β受体的Kd为1nM,结合位点数为500个/细胞。另有报道,用125I标记的受体拮抗剂进行受体分析表明,小鼠淋巴细胞上受体为β2亚型,其Kd=0.9nM,受体密度为3000个/细胞。用24株近交系小鼠进行的受体分析表明,T和B细胞上β2受体动力学参数基本相同,亦不受性别影响。 大鼠腹腔肥大细胞膜上有β受本分布,Kd为1.58±0.56nM,结合容量为4000±14000个/细胞,药理学分析表明,这些β受体中83.5%为β2,而16.5%为β1亚型,且用IgE致敏或相关Ag刺激肥大细胞均不改变β受体的特性。静止的肥大细胞以β受体激动剂刺激15秒,胞内cAMP即有明显的增多,但不影响IgE介导的组织胺的释放。年轻大鼠的脾实质细胞有β2和β2受体的共存。 家兔外周血淋巴细胞的β受体密度为3500左右/细胞,其Kd为0.35±0.18nM。 人外周血淋巴细胞、多形核白细胞、单核细胞、巨噬细胞及血小板上均有肾上腺素能受体。正常人和哮喘患者淋巴细胞上β受体密度有异,而受体亲和力不变,服用β受体激动剂可降低β受体密度,呈下调现象。正常自愿受试者每天服用terbutaline 6mg,7天后淋巴细胞上β2受体数目减少42%。T和B淋巴细胞的受体参数无明显差异。血小板上有α肾上腺素能受体,刺激其受体可促进血小板聚集。人多形核白细胞及Mφ上有α2受体的存在。另据新近报道,慢性感染患者外周血中单个核细胞的β2受体密度与血清中可溶性IL-2受体的水平有关。 (2)多巴胺受体:小鼠和大鼠淋巴细胞膜有多巴胺受体,其Kd分别为4.8±0.2nM和1.9nM。小鼠B淋巴细胞上的受体密度为60000个/细胞,且多种抗多巴胺药物均可抑制放射性配基与多巴胺受体的结合。 (3)ACh受体:以同位素标记的M受体可见于小鼠脾淋巴细胞和非淋巴细胞上,前者是的Kd为1nM,密度为200个/细胞,后者密度为400个/细胞。小鼠胸腺和家兔胸腺细胞的胆碱能受体为N型,可特异地结合银环索毒素,提示胸腺的部分细胞可能起源于神经嵴或神经外胚层。骨髓干细胞膜上的ACh受体参与干细胞的激活。另外,Jurkat细胞株具有M3型的ACh受体,M3受体激活后细胞内Ca2+浓度上升,这一效应系PLC和IP3所介导的。Jurkat细胞膜上M3受体的Kd为14.1nM,最大结合为45370位点/细胞,所制备细胞膜也具有这一结合活性。 (4)5羟色(5-hydroxytryptamie,5-HT):5-HT既是神经递质,又是免疫细胞如肥大细胞和嗜碱性粒细胞的活性分泌物。已发现激活的人T细胞膜上有5-Ht 1a受体的分布,此受体的激活可增加胞内cAMP尝浓度。人T淋巴细胞系Jurkat也表达5-HT1a受体,其作用可由IP3和Ca2+介导。 (5)组织胺(histamine)受体:人T细胞有Kd为0.4nM及数目为35000/细胞的组织胺受体。CD8+T细胞上的组胺受体为H2型,其密度约为6000-7000/细胞,并受白细胞介素和H2受体拮抗剂西米替丁的调节。B细胞上的组织胺受体亦以H2型居中多。 2.类固醇激素受体 分子生物学研究工作表明,几种类固醇激素的胞内受体构成一受本超家族,包括糖皮质激素受体(glucocorticoid ,receptor,GR)、雄激素受体(androgenreceptor,AR)、孕激素受体(progesterone receptor,PR)、盐皮质激素受体(mineralocorticoid,receptor,MR)、甲状腺激素受体(thyroidhormone receptor,TP),视黄酸受体(retinoicacid receptor,RAR)及维生素D受体(vitaminD erceptor,VDR)。其中GR、MR、AR和PR均可识别和结合DNA分子中一段基因序列,称之为糖皮质激素反应原件(glucocorticoid response element,GRE),其序列为AGAACAnnnTGTTCT由GRE介导可影响靶基因的转录。 (1)GR:GR广泛分布于多种淋巴组织及器官,存在于免疫细胞的胞浆及核内。GR在免疫细胞的表达有如下特点:①有较大的性别差异,如雌鼠胸细胞内GR浓度低于雄鼠。②抗原刺激及PHA均可上调GR浓度,而地塞米松则使其下调。③Ca2+参与对GR失活速率的调控。④IL-2及IL-4联合应用可降低人外周血单个核细胞GR对配基的亲和力,并使其增加,此作用可被IFN-γ阴断。⑤LPS可促进GR在小鼠Mφ的表达。 GR由800多氨基本组成,其序列可分为几个功能区域:①DNA结合区,由80氨基酸残基构成,中心部分为两上锌指结构,可结合DNA双螺旋的大沟(major groove)内;②C端为糖皮质激素(GC)结合区;③N末端有Tau1区,可在GR与DNA结合后,以反式激活靶基因的转录。此外,在GC结合区邻近,也有Taul区,参与GR在核内转位。无配基存在时,GR与300kDa的蛋白复合物结合而处于无活性状态。此蛋白复合物由2个亚意念的90kDa热休克蛋白(HSP90),59kDa的免疫亲和素(immunophilin)及其它抑制性蛋白组成,HSP90结合于GR的C末端,参与GR的折叠构型并防止其自胞浆向核内转位。免疫亲和素也可结合CsA、FK506及rapmycin等免疫抑制剂,提示GC的免疫效应与其它免疫抑制剂的作用机制可能类同。 (2)AR:已证实在大鼠、小鼠的胸腺及鸡的法氏囊上皮细胞内有睾酮受体存在。 (3)ER及PR:雌二醇(F2)受体存在于大鼠、小鼠、牛及人的胸腺中,其Kd约为0.2nM,可能定位于胸腺上皮细胞或网状细胞内。鸡法氏囊也有E2受体。PR则见于大鼠胸腺细胞内。 3.神经肽及肽类激素受体 (1)ACTH受体:已知小鼠脾细胞膜上有高亲和力和低亲和力两种ACTH受体,其Kd分别为0.1nM和4.8nM,受体密度为3000/细胞及5000/细胞。人外周血单个核细胞也有此两种受体,Kd值分别为0.04M和3.4nM。免疫细胞上的ACTH受体与肾上腺皮质细胞膜的ACTH受体性质和结构基本相同,其分子量为225kDa,由4条多肽链构成,分子量分别是83、64、52和22kDa。 (2)GH受体:小鼠及小牛胸腺细胞,人T细胞、外周血单个核细胞均有GH受体分布。胸腺的GH受体密度为10-20000/细胞,而IM-9淋巴母细胞系细胞膜上GH受体的Kd为1.3nM,密度为4000/细胞。 (3)PRL受体:PRL与GH对免疫细胞作用广泛,故其各自受体亦应存在于免疫细胞膜上。人外周血T及B淋巴细胞PRL受体Kd=1.66nM,密度为360/细胞,由E2所致的大鼠淋巴瘤Nb2株细胞的PRL受体Kd为75pM,每个细胞有12000个结合位点。另发现,环孢霉素A能增加淋巴样细胞对125I-PRL的结合。 (4)阿片肽受体:阿片肽受体不同的亚型及非阿片样受体均存在于免疫细胞膜上。人外周血淋巴细胞和血小板可结合3H-纳络酮。非阿片肽受体主要与β-内啡肽(β-endorphn,β-END)的C端相结合,参与调节淋巴细胞对植物血凝素的反应。 (5)SP受体:利用放射受体分析、放射自显影及FACS等技术已证实SP特异性受体分布广泛,如大鼠脾脏富含B细胞的边缘区,小鼠脾脏及肠壁Peyer氏结中的T和B细胞,豚鼠腹腔巨噬细胞等(表10-2)。 表10-2 SP受体在免疫细胞上的颁布及特性
注:在速激肽受体中,SP受体为NK-1型,系G蛋白受体家族成员之一。 (6)其它:CD4+T细胞膜上有与腺苷酸环化酶相偶联的VIP受体。降钙素受体分布于人外周B细胞膜上,提示降钙素不但能调节骨骼生理过程,还可影响免疫功能。同样,LHRH、促肾上腺皮质激素释放激素(corticotropin-releasing hormone,CRH)、CGRP、ANP、心房利钠肽(atrial natriuretic polypeptide,ANP)、血管紧张素Ⅱ(angiotensin Ⅱ,AⅡ)、VIP、SS等受体也见于免疫组织及免疫细胞上。 4.褪黑素受体 目前发现,在鸡、鸭等家禽及鹌鹑的胸腺、脾脏、淋巴结和法氏囊等部位可特异性结合褪黑素。褪黑素具有脂溶性,可穿透胞膜而作用于胞浆及核内受体。 (三)免疫细胞合成的神经肽或激素1.POMC族肽 前阿黑皮素(proopiomelanocortin,POMC)为促肾上腺皮质激素(adrenocorticotropin,ACTH)的前体分子,也是β-LPH(促脂激素)、α-MSH(黑素细胞刺激素)及β-END的前身。人外周血淋巴细胞及脾细胞在病毒感染及LPS作用下,可分泌ACTH和β-END,与垂体分泌的ACTH和β-END结构一致。小鼠脾脏中部分Mφ及大鼠某些淋巴细胞则稳定生成这些激素,POMc mRNA可表达于Mφ及淋巴细胞中。在PHA刺激下,人外周血细胞中POMc mRNA表达增强。LPS刺激小鼠脾细胞,亦使其胞浆中POMC mRNA增多。小鼠白细胞对不同的刺激反应各异,如以CRF或新城病毒加入培养液中,则白细胞分泌的POMC肽类以ACTH(1-39)和β-END(1-31)为主,而LPS引起白细胞主要生成ACTH(1-25)和β-END(1-16,1-17)。有人将β-END归为细胞因子。 2.TSH 已证明人外周血B细胞在SEA刺激下可分泌TSH。Molt-4是人T细胞性白血病细胞株,能稳定生成TSH,其化学结构与重体中TSH相同。 3.GH及PRL Con A可提高淋巴细胞中GH及PRL的mRNA水平。T及B细胞也可稳定生成GH,其分子量为正常或高分子量。在造血及淋巴组织,IM-9淋巴母细胞系及Jurkat细胞存在有控制GH和PRL表达的转录因子Pit-1/GHF1 ,这些细胞亦含有GH及PRL的分子及mRNA,因此,GH可以旁分泌方式调控淋巴细胞和造血细胞的增殖和分化。GH在这些细胞中的合成及分泌可能主要受局部生长因子及类固醇激素的调控。 4.SP 人嗜酸性粒细胞可合成SP。血吸虫所致的小鼠肝脏肉芽肽中嗜酸性细胞也能合成SP。 5.VIP及SS 在血小板、单个核细胞、肥大细胞及单核细胞中均发现有VIP或SS的免疫阳性物质分布。 6.LHRH 大鼠脾脏及胸腺的淋巴细胞中含LHRH及其mRNA,免疫细胞中mRNA的序列与下丘脑中存在的LHRh mRNA的的序列相同。Con A可刺激LHRH在T淋巴细胞的合成,PHA亦有类似作用。新近发现,人外周血中CD4+及CD8+T细胞可表达LHRH及其mRNA,表达水平受细胞状态的影响。 7.CRH CRH及CRH mRNA存在于大鼠胸腺和脾脏中,且与下丘脑中CRH及其mRNA结构及序列相同。胸腺和脾脏中的CRH含量与下丘脑相比为1.7:1:117。CRh mRNA主要表达于胸腺及脾脏中的淋巴细胞内。这些细胞的CRH分泌不受IL-1的影响,但脂氨化酶抑制剂则可加强CRH的分泌,这些特征与下丘脑CRH的分泌调节不同。人外周血淋巴细胞和中性粒细胞也有CRH分子及其mRNA的表达。在大鼠炎症组织如风湿性关节囊滑巴细胞和中性粒细胞也有CRH分子及其mRNA的表达。在大鼠炎症组织如风湿性关节囊滑膜组织中亦检测出CRH的分布。以上事实提示CRH可以旁分泌或自分泌的方式参与免疫调控。 8.其它 胸腺上皮细胞还可合成精氨酸血管加压素(arginine vasporessia, AVP)及催产素(oxytocin, OT)。GHRH在大鼠白细胞中的合成亦得到证实。
二、激素、神经肽及神经递质对免疫功能的影响激素、神经肽及神经递质等神经内分泌信息分子可借经典内分泌、旁分泌和自分泌途径,影响或调节免疫应答,并能与某些免疫病理过程。 (一)类固醇激素1.糖皮质激素(GC) GC对免疫功能的影响极为广泛。Selye等于1936年首先观察一肾上腺皮质提取物可导致大鼠胸腺萎缩。其后证明GC可通过多种途径影响免疫系统,且此效应存在较大的种属差异,如小鼠、大鼠、仓鼠和兔较为敏感,而豚鼠、猴和人相对不敏感,主要差异表现为后者的淋巴细胞不易被GC作用反致溶。 (1)GC影响胚胎期免疫系统的发育:如小鼠胚胎胸腺在GC作用下,其淋巴细胞表达Thy1.2抗原增加,而高浓度的GC可杀伤小淋巴细胞。胸腺的上皮细胞对GC尤为敏感。GC引起胸腺萎缩的机制涉及细胞程序性死亡或凋零(apoptosis),此作用需要核酸内切酶的参与,在Ca2+及Mg2+激活核酸内切酶,后导致DNA的断裂。GC明显降低胸腺激素的分泌水平,减少胸腺中胸苷激酶(TK)的活性。离体大鼠胸腺细胞接触Gc 4小时后,胞浆中RNA降解速率加快。另外,胸腺细胞不同发育阶段对GC的反应有所差异,如人胚胎胸腺中,胸腺前体细胞对GC的敏感性较成熟细胞为高。 (2)GC影响淋巴细胞的生成和骨髓造血机能:如减少骨髓中成熟B细胞数目,提高髓髓中Mφ及粒细胞的集落形成率。 (3)GC改变细胞的循环和重新分布:小鼠给予GC后,血中单个核细胞及嗜酸性粒细胞减少。GC可降低淋巴细胞自血中进入淋巴结的数量,但促进淋巴细胞空过血管内皮而进入骨髓腔。 (4)GC对淋巴功能的调节作用:①GC可降低PHA引起的T细胞增殖以应,这可能与降低IL-2R表达有关。GC还能减弱T细胞的趋化及游走性,抑制脾脏中的B细胞对LPS及PPD的反应,减少Ig合成细胞的数目,改变PWM诱导的PFC形成率。②在GC作用下Mφ的APC功能受抑制,且IL-1分泌减少。GC也抑制单核细胞转变成Mφ,抑制皮肤Langerhans细胞的功能,削纯收益Mφ的吞噬及细胞内杀伤能力。③调节NK细胞的功能,如小鼠脾细胞培养中NK细胞活性受地塞米松(10-7-10-11M)的抑制。体内药理剂量的GC则减少脾脏中NK细胞数目,但也有相反的报导。 (5)GC对肥大细胞功能的影响:GC抑制Ag所致肞大细胞脱颗粒反应,减少组织胺的释放,减少嗜酸性粒细胞数目,抑制其趋化反应,降低粒细胞的渗出和吞噬活动,并能对抗某些细胞因子维持嗜酸性粒细胞的存活作用。 (6)GC对细胞因子产生及生物活性的影响:GC在风湿性关节炎患者可抑制IL-1引起的IL-6基因表达;减弱LPS诱导的TNF-α产生,增加IL-α、IL-1β及IL-6mRNA的不稳定性,减少IL-2的分泌,与GM-CSF联合应用可提高中性粒细胞对IL-1的结合,与造血生长因子协同诱导骨髓细胞表达IL-1受体GC通过阻抑IL-2R的信号传递。降低免疫细胞对IL-2的反应性。GC受体拮抗剂RV38486能模拟IL-1作用而加强TNT-α的致死及诱生IL-6效应。GC还可对抗IL-1β对胰岛素分泌的抑制效应。 (7)GC对MHC I类及Ⅱ类分子表达的抑制作用:MHC参与T细胞识别粘附及APC功能,MHC表达过低或不表达,可引起严重的免疫缺陷,而表达过高则可纠起血身免疫性疾病。现已证明,GC可抑制小鼠B细胞和巨噬细胞MHc Ⅱ基因I-Aβ的激活。GC的部分免疫抑制效应是由脂皮素(lipocoritin)介导的,脂皮素是由至少6种蛋白质构成的家族,其结构与细胞骨架和胞吐相关蛋白(calpactin)类似。在GC作用下,大鼠腹腔白细胞、人羊膜细胞、人外周血单个核细胞及人支气管肺泡冲洗液中Mφ等的脂皮素生成增加。而摘除肾上腺可减少大鼠几种组织内脂皮肤mRNA及蛋白水平。GC主要影响脂皮素1和2的含量,使胞浆中及与胞膜相关的脂皮素1和2浓度升高。脂皮素具有较强的抗炎和免疫抑制效应,如抑制PAF及类花生酸等的合成,并模拟GC的众多作用。在类风湿性节炎患者,脂皮素1自身抗体的存在GC的反应性缺损有关。 (8)GC对粘附分子表达的调节作用:GC的另一免疫调控机制涉及ELAM及ICAM。GC可抑制血管内皮细胞表达ELAM-1及ICAM-1mRNA和蛋白分子,此作用可被GR拮抗剂RU486所阻断。GC可调节白细胞的循环及定缶滪和游走反应,从而发挥其强大的抗炎和免疫抑制效应。 (9)GC对某些酶合成的调节作用:GC还较强地抑制成纤维细胞合成胶原酶,抑制多种磷脂酶的合成,影响某些金属蛋白酶的表达,促进血管紧张素转换酶(angiotensin-converting enzyme,ACE)及中性肽链内切酶(neutralendopeptidase,NEP)的生成,ACE和NEP可分别降解缓激肽及速激肽等炎症介质。在哮喘及结肠炎症性疾病时,局部组织的速激肽受体NK1表达增高,并可介导SP的免疫调节及致炎作用。此受体的表达亦受GC的抑制。 (10)GC对MO产生的调节作用:NO作为细胞内及细胞间信息分子也参与免疫反应,如促进炎症组织的血浆外渗。催化NO合成的酶为NO合成酶(NOS),其表达受细胞因子的调控。现已证明GC可阴抑NOS的基因转录,从而减少NO的合成和释放。 目前发现, GC对免疫功能的调控不仅仅是抑制性的,在某些实验条件下,较人氏剂量的GC可增强淋巴细胞的增殖反应。 近年来,对GC的作用机理已有了分子水平的认识。GC结合于无活性GR后,使GSP90及immunophilin等蛋白与GR解离,有活性的GR即可识别糖皮质激素反应元件(GRE)序列,由于GRE位于GC靶基因的启动子区域,故可诱导或阻抑靶基因的表达。GRE的数目及相对于转录起始上点的位置可能决定GC影响转录的程度,GC阻抑某些靶基因转录的机制可能和阻抑性GRE有关,GR与此类GRE结合后,以空间位阻方式抑制其它转录因子的促转录作用。新近发明,GR还可直接作用于某些转录因子,从而发挥鞭抗炎效应,如转因子AP-1(激活蛋白-1)是由Fos蛋白及Jun蛋白组成的二聚体。AP-1促进胶原酶基因的活化。有活性的GR可结合于AP-1从而抑制胶原酶的合成。AP-1还参与T细胞的活化,促进IL-2及IL-2R基因的表达等,GC则通过GR的活化而AP-1的活性以对抗细胞因子的作用。其它转录因子如NF-κB及NF-AT等也受GC的负性调控。此领域的研究将对合理的药物设计及相关的临床实践具有指导意义。 2.龙激素 一般而言,睾酮等雄激不经对免疫功能有抑制性作用。睾酮可减少人泪腺中IgA的产生,这一作用为雄激素所独有。在睾酮的作用下,胸腺的重量和体积均减少。小鼠迟发型皮肤超敏反应及抗体的生成亦受睾酮的抑制,去势可逆转这些变化。睾酮还可降低实验动物对许多细菌、支原体、寄生虫及病毒感染的抵抗力,表现为感染后的致死率及肿瘤发生率明显升高,去势为着能逆转这些改变。 与孕酮及E2相反,睾酮阻抑乳腺上皮细胞表达Ia分子。此外,IM-9系淋巴细胞膜上SP受体(NK1受体)的睾酮的作用下Kd值增大,提示睾酮对SP这一神经源性炎症介质的作用有一定影响。 3.雌激素 雌激素可提高体液免疫力而减低细胞免疫机能。 (1)对体液免疫功能的影响:E2促进子宫分泌IgG,也使子宫内膜上皮细胞的IgA含量增加。C57BL小鼠接受雌激素后,针对SRBC的溶血性抗体滴度上升,面C3H小鼠无此反应,提示该作用存在品系差异。 (2)对细胞免疫功能的影响:雌激素制剂能降低胸腺重量,减少胸腺中淋巴细胞数目,但可增加脾脏的重量及脾细胞数。生理条件下,雌性小鼠的脾细胞数目也较雄鼠为多。在去卵巢的雌性大鼠,E2可引起胸腺萎缩。E2还能强烈地抑制PHA及ConA等高层的大鼠胸腺细胞增殖反应。E2抑制小鼠及人的外周血T淋巴细胞DNA的合成,E2还降低NK细胞的活性,减弱poly I-C及短小棒状杜菌对NK细胞的刺激作用,同时增加小鼠实验性或自发性肿瘤的发生率及转移率,延长同种异体皮肤移植物在小鼠的存活时间。去垂体大鼠给予PRL可恢复免疫功能,而同时切除卵巢后,PRL不足以完全恢复免疫功能,必需合用E2方可秦效。FE尚能提高肥大细胞的数目,刺激肥大细胞的功能。 4.醛固酮 醛固柄借胞膜受体而快速影响人单个核白细胞的Na+交换,从而改变细胞内的高子尝试及细胞体积,其机制可能与IP3的生成有关。 (二)甲状腺激素甲状腺激素对体液免疫和细胞免疫均有促进作用。新生及年轻大鼠去甲状腺后,将引起外周血淋巴细胞数目降低,抗SRBC的抗体反应下降,脾细胞对PHA刺激的增殖反应减弱,这些效应有一定的时间依赖性,即新生大鼠去甲状腺后的上述变化发生于断乳后,而年轻大鼠亦需经40-60日显类似改变。可见,甲状腺对免疫机能有正性调控作用。遗传性免疫缺损的Snell-Bagg小鼠给予生长激素(GH)及T4后可重建其免疫功能。T3可能增加幼龄小鼠胸腺上皮细胞数目,并增大髓质体积。长期给予T4可提高外周血淋巴细胞数量,特别是T细胞数目。在小鼠及人,甲状腺激素均促进淋巴细胞对丝裂原的增殖反应,并有明显的剂量依赖关系。 (三)蛋白质及肽类激素1.GH 人的GH由191个氨基酸残基组成,不同种属的GH结构和活性有较大的差异。GH是腺重体激素中极重要的免疫调节因子。GH受体是红细胞生成素(EPO)受体超家族的一员,GH既可借助受体直接影响免疫细胞的功能,也可由胰岛素样生长因子(insulin-like growth factor,IGF)的介导而间接作用于免疫细胞,因GH诱导IGF的生成,且IGF-I受体分布于所有外周血单个核细胞膜上。GH可影响免疫系统的各个环节,其中胸腺为其主要的靶器官。 (1)小鼠去垂体后胸腺体积和重量减少,淋巴组织萎缩,DNA合成减少,由抗原诱发的抗体反应减弱,脾脏中NK细胞活性下降。大鼠去垂体后素现为胸腺和淋巴结的增殖反应减弱,脾脏中DNA代谢速率慢,皮肤移植后排斥反应受抑制,难以诱发佐剂性关节炎,且抗体合成锐减。给予GH则可逆转去垂体后的上述变化。 (2)儿单期重体功能低下引起侏儒症,伴有贫血及EPO降低。以GH治疗则促进生长,增加骨髓中淋巴细胞的数目并加速血,尿中EPO含量也增高。 (3)隐生遗传性垂体性侏儒小鼠(Snell-Bagg小鼠)的免疫机能较差,突出表现为胸腺退化早,外周淋巴组织及骨髓中细胞稀少,免疫反应性降低等。以GH及T4联合处理此株小鼠,可防止胸腺萎缩,提高淋巴细胞数目,恢复免疫机能。GH的这一作用可能是由胸腺介导的,因去胸腺后GH促进免疫功能的作用消失,现已发现GH能促进胸腺激素的释放。 (4)衰老时,GH分泌减少,免疫功能降低。结予GH媃中恢复免疫功能,促进胸腺激素的分泌,可速T细胞前体进入胸腺,并处长衰老小鼠的寿命。分泌GH的GH3垂体瘤细胞移植也可增加胸腺体积和胸腺细胞数目。 (5)GH促进正常人T细胞集落的形成,并刺激淋巴细胞的增殖。GH可加强PMA对单个核细胞释放H2O2的刺激效应。GH还可加强单个核细胞的趋化活性,此作用可被SS所拮抗。Mφ在GH刺激下对低密度脂蛋白(LDL)的摄取和降解加速。新近报道证明,重组GH可直接刺激B细胞增殖及分泌Ig。 基于上述事实,有人提出可应用GH治疗骨髓功能衰竭、免疫功能低下以及抗衰老。 2 .PRL PRL存在于所有脊椎动物体内。在低等变温动物,PRL可能主要参与对渗透压、生长、发育和代谢等的调节。而一地哺乳动物及鸟类,PRL与生殖功能密切相关,如刺激哺乳动物乳腺的发育和分泌乳汁,雄性附性器官的生长和分泌,加速雌体的黄体生成及溶解等。在分子结构上,PRL与GH及胎盘催乳素均二盼相似,且PRL与GH的各血特异性受体录属于红细胞生成素受体超家族。同GH相似,PRL也对免疫功能珍有正调节作用。 PRL不仅促进乳腺发育和泌乳,还能提高乳腺中分泌IgA的细胞数目,淋巴细胞游走进入乳腺。母乳中PRL浓度与婴儿血浆IgG及T淋巴细胞数目成正相关,说明母乳喂养是重要的免疫刺激作用。去垂体动物于肾囊下埋植同种异体垂体后,可恢复多种免疫功能,如抗SRBC的抗体形成,对DNCB的接触致每及佐剂性关节炎的发生。已知移植垂体主要分泌大量的PRL,故PRL可能是移植重体恢复免疫力的主要因素,因为单纯给予PRL媃中恢复去垂体动物的免疫机能。反之,向去重体动物注射抗PRL抗血清,则支物发生贫血甚至死亡。抑制PRL分泌的药物也同样抑制动物对DNCB的接触性超敏反应。 PRL的免疫调节作用涉及如下方面:①促进抗体合成;②刺激法氏囊细胞的分裂增殖;③促进胸腺组织的增生,诱导腈胎期胸腺细胞表达Thy-1抗原及T细胞抗原;④与IL-2协同刺激T细胞的克隆增殖,并诱导其表达IL-2R,对克隆的 T细胞L2株系,PRL也与IL-2协同诱导其表达干扰素调节因子(IRF-1),C-myc,ODC(鸟氨酸脱羧酶)、组蛋白及cyclin B等分子,促进T细胞的增殖;⑤刺激大鼠Nb2淋巴瘤的增殖,并抑制Dex引起的DNA断裂,防止及对抗Nb2细胞的Dex作用的凋零;⑥激活Mφ;⑦激活NK细胞,并与IL-2协同诱导LAK活性。 3.ACTH ACTH为39肽,可影响多种免疫细胞。在整体水平,ACTH的效应至少经由二条途径,其一是刺激GC的分泌而间接引起免疫抑制,其二是借助其在免疫细胞膜上的特异受体而直接影响免疫功能。ACTH纯制剂引起胸腺萎缩及脾萎缩,伴有淋巴细胞数目减少,而去肾上腺后此效应仍然存在。 (1)ACTH对B细胞功能的调节:ACTH在体外可抑制T细胞依赖性抗原(如SRBC)及非信号依赖性抗原(如DNP-Ficoll)的抗体反应,减少PFC数目。此作用具有明显的ACTH分子结构特异性,如ACTH(1-39)为抑制性的,而ACTH(1-24)无效。ACTH还可与IL-2或DCGF协同刺激正常的B细胞生长和分化。对BCL1细胞系而言,ACTH可能以自分泌方式促进其增殖。 (2)ACTH对T细胞功能的调节:ACTH抑制T细胞产生IFN-γ,并调节IL-2的生成。新近发现,Jurkat细胞膜上CD3分子的γ链磷酸化过程也受ACTH的负性调控。ACTH能增强混合淋巴细胞反应(MLR)中的细胞毒作用。此外,ACTH能完全阴止IFN诱导Mφ的杀伤肿瘤活性,并抑制腹腔Mφ的MHCⅡ类分子表达。 4.β-END β-END与ACTH来源于共同的前体POMC,由于β-END既能自重体释放,也可在免疫细胞中合成,且其受体广布于多种免疫细胞,故β-END具有广泛的免疫调节作用。 (1)β-END对T细胞的影响:β-END可促进T细胞的增殖反应,但也有相反报道。β-END还能抑制T细胞表达IL-2R,抑制人外周血T细胞(HPBTL)的玫瑰花环形成率,改变T细胞膜上CD3原的表达,影响PHA引起CD3γ链的磷酸化以及干扰CD3-TCR复合物的内化过程。 (2)β-END对其它免疫细胞的影响:β-END以剂量依赖方式促进NK细胞的细胞毒作,并可活化Mφ促进其吞噬和趋化活性,并可调节MHC Ⅱ类分子的表达。 除β-END外,α-END,γ-END强啡肽(dynorphin),M-ENK及L-ENK等阿片肽类均可借助各种阿片样受体调节免疫细胞的功能。 5.CRH 作为41肽的下丘脑激素,CRH至少经由二条途径影响免疫机能:CRH可单独或与AVP协同刺激ACTH的释放而激动GC的分泌,后二者均具有广泛的免疫抑制效应;CRH借助免疫细胞膜上的受体而直接影响免疫细胞。鉴于CRH可由胸腺及脾脏等免疫器官合成,故CRH可能具有重要的生理性免疫调节作用。CRH抑制人外周血单个核细胞分泌IL-1β及IL-6,CRH可能首先抑制IL-1β的生成,引起IL-6继发性分泌减少。妊娠时CRH及GC的血浆中浓度均升高,故可能抑制母体对胎我的免疫反应。 也有文献报道了CRH的免疫增强作用,CRH可刺激人外周血单个核细胞分泌IL-6,抑制IFN-γ的分泌,但不影响此类细胞的增殖及IL-1β的分泌。有报道nM水平的CRH能刺激人外周血单个核细胞分泌IL-2及IL-1,增强LPS及PHA分别对IL-1及IL-2的促分泌反应,刺激β-END的分泌。CRH亦能促进淋巴细胞的增殖,IL-2R(Tac)的表达水平,并可调节NK细胞介导的杀伤细胞作用。 6.LHRH 胸有少脾脏不仅含有CRH及其mRNA,也有CRH的受体表达,且此类受体直接分布于大鼠及小鼠的淋巴细胞上。目前认为,胸腺可能是衰老的时钏。老龄大鼠胸腺重量呈进行性减轻,同时伴有CRH受体数目的减少,而给予CRH强效类似物(LHRHA)可逆转这些改变,并在单用或合用ConA时促进胸腺细胞的增殖反应,刺激IL-2R的表达。LHRH-A主要影响CD4+或CD8+T细胞亚群。雄鼠去势也可引起类似变化,如再给予LHRH-A则呈协同作用。LHRH在体内或体外均具有促进免疫功能的作用。 7.SP 在从多神经肽中,SP的免疫调节效应研究最为广泛和深入。SP可影响所有的免疫细胞。 (1)SP对人外周血淋巴细胞的作用:SP有剂量信赖性的促进淋巴细胞增殖效应,并加强ConA及PHA的刺激反应,SP受体拮抗剂可抑制此反应。因此SP可能是T细胞的丝裂原或辅助丝裂原。SP还可刺激小鼠脾淋巴细胞、肠壁Peyer氏结及肠系膜淋巴结淋巴细胞的增殖。SP及其N端片断SP1-4可防止大鼠应激所致的胸腺萎缩,在对镍过敏的个体,SP加强硫酸镍的促T淋巴细胞增殖效应。另有发现,SP不依赖受体介导亦能升高人T细胞内Ca2+浓度。 (2)SP对B细胞的作用:SP促进B细胞分泌Ig的报道较为一致。SP刺激体外培养小鼠Peyer氏结、肠系膜淋巴结及脾脏来源的B细胞IgA的合成分别增加约300%、50%及70%。体内给予SP1-7日后,上述三种组织的淋巴细胞在培养时IgA及IgM的合成明显增加,此作用为生理性的,因所用SP剂量在生理波动范围内。SP对IgA合成的影响最明显,提示SP参与调节憉部免疫。 (3)SP对单核-巨噬细胞的作用:SP既能促进其吞噬和趋化游走活性,又可刺激其的氨化爆发反应(oxidative burst),促进多种介质的释放,且所需DP尝试较低。如小鼠腹腔Mφ及人外周单核细胞的SP及SP1-4作用下吞噬功能增强,SP刺激豚腹腔Mφ的有氧呼吸,加强花生四烯酸的代谢,生成和放出O2-、H202、TXB2、PGE、6酮PGF1α、LTC4及溶酶体酶ADGase(β-D-2-乙酰氨-2-脱氧葡萄糖苷酸酶)等,SP促进人外周血单核细胞释放IL-1、IL-6及TNF-α,促进IFN-γ的合成与分泌,诱导小鼠Mφ细胞系P388D1细胞释放IL-1,SP可还与M-CSF协同刺激小鼠骨髓单核-巨噬母细胞系的增殖反应。通过以上作用SP间接地调节Mφ与T细胞间的识别、抗原加工及提呈等过程。 (4)SP对中性粒细胞及嗜酸性粒细胞作用:SP在生理浓度即可刺激人多形核白细胞的趋化运动,明显增强C5a 所致的中性粒细胞趋化、游走运动及吞噬杀菌活性。SP还能促进中性粒细胞粘附于支气管上皮细胞,故可能参与呼吸道的病理过程。此外,SP可通过肥大细胞而促进粒细胞的浸润。SP对嗜酸性粒细胞的影响不甚明了,但SP同样由肥大细胞脱颗粒而吸引嗜酸性粒细胞的渗出和游走,缺乏肥大细胞的WBB6F2-W/Wγ及WCB6F2-SL/SL2系小鼠无此反应,而当这类小刀竕别移植同种骨髓细胞或局部注射小鼠肥大细胞后,皮下给予SP即可引起该部位的嗜酸性粒细胞的渗出反应。 (5)SP对肥大细胞的作用:在人及多种实验动物均证明了SP刺激肥大细胞释放组织胺的效应。SP不促进5-HT自大鼠肥在细胞的分泌。SP诱发组胺及5-HT释放反应十分迅速,30秒内释放量可达最大值的90%,并依赖于糖酵解和氧化磷酸化过程。SP的这一作用是由G蛋白介导的,不需要胞外Ca2+的存在,也不引起IP3及DAG的含量变化,且IgE诱发的组胺释放与SP的效应间无交叉脱敏现象。肥大细胞能表达及分泌许多细胞因子,如TNF-α、IL-1、IL-3、IL-4、IL-6和GM-CSF等,SP则选择性地促进肥大细胞系CFTL12表达TNF-αmRNA及释放TNT-α。上述作用表明SP对肥大细胞的影响与过敏疾病的发生和发展有密切的联系。 (6)SP对其他细胞的作用:SP促进成纤维细胞、滑膜细胞等结缔组织细胞的增生,并协同IL-1的致成纤维细胞增殖活性,并可刺激其释放胶原酶及PGE2。险些,SP诱发肥大细胞分泌组胺,从而引起血管扩张、血浆外涌及炎性细胞浸润,导致局部充血水肿。在溃疡性结肠炎、十二指肠溃疡、类风湿性关节炎及佐剂引起的实验性关节炎等病变部位,SP含量明显升高,胸膜腔炎性渗出液中及家兔内毒素休克时血中SP浓度也上升,这些事实均提示SP作为一种炎性介质参与重要的免疫病理过程。 8.血管紧张素Ⅱ(AⅡ) 对AⅡ的免疫调节效应了解不多。已证明AⅡ刺激人外周血单核细胞氧化爆发反应,增强其胞内伤能力,但不影响其化学趋性,低浓度AⅡ(10-9M)的作用由对百日咳毒素(PTX)敏感的G蛋白介导,引起胞浆中Ca2+浓度上升;而高浓度的AⅡ(Ca-6M)引起Ca2+内流加速,PLA2活性增强,刺激花生四烯酸的代谢及促进PKC的移位。 9.SS SS可使大鼠灌流肝脏Mφ的胞饮活动增强,并以温度及Ca2+依赖方式刺激大鼠腹腔肥大细胞释放组胺。SS还能对抗VIP引起的大鼠淋巴细胞中腺苷酸环化酶活性增加。 10.FSH(卵泡刺激素follicle-stimulatinghormone)及LH(黄体生成素,luteinizing hormone)胸腺外皮质层有LH免疫阳性细胞的分布,而在其内层皮质和髓质有FSH免疫阳性细胞的分布,提示LH和/或FSH可能参与胸腺细胞的发育和功能。 11.胰岛素 在小鼠,胰岛素可改变ConA引起的淋巴细胞增殖反应,与LPS联合应用可增加抗体形成细胞数目,胰岛素在不改变血糖浓度剂量时能加强小鼠过敏性休克的发生,并抑制角叉菜胶所致的足垫的肿胀。在人体,胰岛素可促进MLR中的DNA合成,抑制ADCC功能。生理尝试的胰岛素即可加强单核细胞的纤溶性,促进其对静止颗粒的吞噬,并提高多形核白细胞的趋化活性。 (四)经典神经递质1.儿茶本分胺 从支配淋巴器官的神经末梢释放的去甲肾上腺素(NE)及肾上腺髓质释放的肾上腺素(Adr)和NE,经由α及β受体影响各种免疫细胞及免疫功能。儿茶酚胺的作用复杂多样,报道不尽相同。异丙肾上腺素可引起小鼠胚胎胸腺细胞表达Thy-1抗原。Adr可降低人T淋巴细胞对丝裂原刺激的增殖反应,降低体液免疫应答,导致抗体合成减少及I型超敏反应受抑制。对吞噬细胞影响的研究结果不一致,如Adr和NE在生理浓度时抑制Mφ分泌IL-1,而另有报道称α2受体兴奋促进Mφ释放TNF。Adr和NE抑制吞噬细胞的趋化游走及吞噬活性。儿茶酚胺还降低移植排斥反应,改善GVHR。新近发现,儿茶本分胺还可作用于脑血管内皮细胞,促进MHc I及类Ⅱ类分子表达,但NE季节低人星形胶质细胞瘤MHCⅡ类分子的表达。 2.ACh 胆碱能药物如氨甲酰胆碱(carbachol)可升高人外周血T细胞的E花环形成率,此反应可被阿托品所阻断,说明有M受体的参与。Ach还经由M受体提高大鼠T淋巴细胞的细胞毒作用,促进PHA所致的淋巴细胞转化和蛋白质合成。在离体人肺组织,ACh刺激组胺的释放,此效应亦受阿托品的拮抗。低剂量的ACh直接刺激肥大细胞释放组胺。ACh参与肠敏反应的发生,如牛乳中含β-乳球蛋白,可引起对牛乳的过敏反应。β-乳球蛋白能诱发迷走末梢释放ACh,可为肠道内源性免疫介质。 3.5-HT 5-HT即可作为神经递质,亦可由血小板及肥大细胞释放。5-HT能解除T细胞增殖的抑制因素,影响NK细胞活性,抑制Mφ表达Ia分子。 4.褪黑素 松果体与免疫功能与有密切的联系。以药物阻断松果体的功能、摘除松果体或动物连续光照等措施,均显著减少初次抗体合成反应及抑制混合淋巴细胞反应。而经予褪黑素可逆转这些变化。褪黑素还可促进小鼠脾细胞生成IFN-γ。
三、应激对免疫系统的影响(一)经典的应激概念 各种伤害性刺激引起的一系列非特异的定型反应均可称为应激,表现为下丘脑-垂体-肾上腺皮质轴系(HPa axis)及交感神经-肾上腺髓质系统的兴奋,并伴有众多组织和器官的功能变化。应激不仅取决于外界环境因素的变动,还肥个体心理因素的影响。 构成应激性刺激的内外环境因素,可分为躯体性为主的、以心理性为主的及混合型三类(表10-3)。 表10-3 应激时血浆中激素水平的变化趋势
注:部分引自徐仁宝(1991) (二)应激对免疫系统的影响 十余年来,应激对免疫系统的影响倍受重视。动物实验及人体观察证实,应激对免疫的影响主要是抑制性。 (1)以电击作为痛性应激刺激,可降低大鼠淋巴细胞对PHA的增殖反应,这一作用有明显的组织差异,如脾脏淋巴细胞较易对电击刺激发生适应。电击还可减弱脾脏中NK细胞活性,抑制Mφ生成H2O2。这些改变主要是由阿片样受体介导的。 (2)以2-脱氨葡萄糖(2DG)抑制细胞对葡萄糖的氧化和利用作为代谢性激模型,也获得类似结果。此应激反应可减少实验性自身免疫性疾病的发生率及其严重程度。 (3)实验动物的饲养条件,特别是每笼饲养动物只数等因素亦明显影响机体的免疫力,如使T细胞依赖性抗体生成减少,T细胞转化率降低。此种影响有种属差异和性别差异,所产生的影响为一过性,的主要影响Th细胞,IL-2的生成,且不依赖于肾上腺的的存在与完整。 (4)应激降低小鼠对HSV感染的免疫力,减少脾脏中细胞毒性淋巴细胞数目,增加小鼠实验性肿瘤的的转移率。 (5)人类外科手朴作为一种典型的应激刺激,可导致血浆中激素和细胞因子浓度的变化,如GH、T4及IL-2等降低,而GC及IL-6升高,这些变化可被PG合成阻断剂消炎痛所阻断,淋巴细胞对PHA的反应降低。儿童脑损伤后,血中淋巴细胞减少,以Th及Ts的减少为最明显,同时白细胞的吞噬能力下降,IgM降低而IgA含量上升。机体缺氧后,首先引起外周血淋巴细胞增多,CD16+细胞增加,NK细胞活性及受刺激后的活性均上升,随后伴有细胞数目的减少。 (6)心理因素对人免疫功能的影响较为显著。如观看外科手术电影构成被动应激,可降低淋巴细胞对ConA的反应,减弱B细胞对PWM刺激的增殖反应,但以进行紧张心算作为主动应激时,仅表现出淋巴细胞对ConA所致的增殖反应下降。孤独感强或易激惹等个性心理特征能明显影响分裂原对淋巴细胞的促增殖反应,同时IL-2R表达水平下降。考试压力及婚姻不和等情感性应激刺激常伴有血中抗HSV、抗EBV或抗巨细胞病毒的抗体滴度上升,CD4+细胞及NK细胞的百分比率及活性也相应降低,提示应激可能降低免疫力,使体内潜伏病毒激活。另外,精神疾患伴有免疫功能失调亦是公认的。 (7)心理性应激与许多人类疾病的发生和发展关系密切。如在回顾性或前瞻仰性调查研究中发现,儿童型糖尿病、Crohn's病、类风湿性关节炎、眼葡萄膜炎、Graves病及上呼吸道感染等疾病与各种心理应激事件有不同程度的关联。这些心理应激事件中,突出的有亲人去世、离婚和失业等生活变故。心理性应激也可能提高肿瘤发生率和转移率。 对应激的可控制或预见性能有效地改善或不出现应激反应。短期应激刺激呈现免疫抑制,而较长期应激则常引起免疫增强。如以声音为应激条件时,小鼠NK细胞活性、淋巴细胞对PHA等的增殖反应即是如此。温和急性的应激训练,可提高淋巴细胞转化水平。 (三)应激影响免疫功能的机理 各种应激引起免疫功能改变的机理较为复杂,举例如下。 (1)CRG-ACTH-GC轴系统的激活。 (2)交感-肾上腺髓质系统的激活。 (3)阿片肽类的参与如,β-END、M-ENK、L-ENK、Dynorphin等。 (4)GH、PRL、α-MSH分泌增加,LH、FSH、TSH(冷刺激除外)等分泌减少,α-MSH可对抗细胞因子激活HPA轴系的作用。 (5)IL-1、IL-6等的释放。 (6)垂体前叶生成的suppressin(暂译抑制素),为63kDa的蛋白质,具有较强的免疫抑制效应,由ACTH、GH及PRL等刺激细胞生成,故可推测其为应激性激素,参与对免疫功能的抑制性调控。 (7)应激时血清中出现多种免疫抑制因子。如手术、烧伤、失血等均刺激机体生成多种血清免疫抑制因子,可抑制淋巴细胞生成IL-2与GC及PGE2等无关。非创作性应激也可引起血清中出现一种免疫抑制因子,其性质为耐热的6kDa的多肽,可抑制正常小鼠淋巴结淋巴细胞的增殖,该因子的生成需中枢神经系统的参与,但不涉及肾上腺素及β-END。 由于应激时众多神经内分泌功能变化,可以多重途径和水平改变机体的免疫力,特别是近年血清免疫抑制因子及腺垂体的suppressin的发现,将有助于阐明应激时神经免疫内分泌相互作用的变化规律及生理或病理意义。如应激时的免疫抑制可保护机体免受更严重的损伤,但另一方面却降低机体对病原体的抵抗力和免疫力,容易引起感染或肿瘤的发生。
四、神经系统定位损毁对免疫功能的影响(一)中枢神经结构损毁的效应 早期有关中枢神经系统影响免疫的工作主要采用于核团及束路损毁技术,如电解损毁、手术切割或化学损毁等方法。在1958年即观察到下丘脑结节部的破环可改变过敏等免疫反应的发生和发展。以后研究进一步发现,中枢神经系统中许多部位损伤后均可引起免疫机能变化,如下丘脑内许多核团损毁,常引起抑制效应,提示这些区域为免疫反应增强区。损毁下丘脑前区后,脾细胞及胸腺细胞的数目减少,抗原及丝裂原刺激所致的淋巴细胞增殖反应减弱,不易发生实验性变态反应性脑炎。小鼠下丘脑腹内侧部、背内侧部及弓状核的破坏导致NK细胞活性降低。啮齿动物的结节漏斗区损伤可促进肿瘤生长。在边缘系统,核团损毁的结果多为免疫增强效应,如乳头体、海马列及杏仁核的破环均表现为提高淋巴细胞的增殖水平,海马破坏还增加胸腺细胞数目。人大脑皮层受损后的免疫机能变化似有某些特点,即左侧皮层损伤伴有脾细胞数目降低,淋巴细胞增殖反应减弱,NK细胞活性下降,但右侧皮层受损则无上述改变,提示大脑皮层在免疫机能调控上的分工及侧化。临床观察说明,左利者易患免疫性疾病也支持上述实验结果。由于单侧皮层损伤后的免疫变化于术后3周消退,这提示可能有某种代偿性机制的存在。鸡胚脑部分切除或损毁可引起胸腺上皮细胞的减少,提示在胚膙发育期,神经系统与免疫系统间即有功能的联系。 以上工作也存在一些特解难题。其一,从方法学角度考虑,中枢结构损毁难以做到高度局限精确,常殃及许多结构和通路,故引起的免疫状态改变很难认为是部位或区域特异的。其二,这些效应的发生途径及机制绝大多数尚不清楚,仅少数资料表明:中脑导水管及颖核损毁后的免疫增强效应系由副交感神经对胸腺的直接支配所介导的;中枢损毁效应不涉及GC,但与重体激素有关。 (二)外周神经损毁的效应 脾神经切除后,小鼠对SRBC刺激的抗体反应增强,新生及成年动物整体给于6-羟多巴(6-OH-OA)可选择性破坏外周交感神经,结果使T细胞非依赖性抗原刺激引起的免疫应答增强。 切除免疫动物单侧的第二颈交感神经节能加强同侧引流区淋巴结的PFC数目,用α-甲基酷氨酸以抑制肾上腺髓质激素的合成则可进一步加强此反应,说明交感神经去甲肾上腺素能系统对免疫的紧张性抑制效应。外周交感神经的免疫调节作用亦存在种属差异,例如小鼠对交感神经损毁所引起免疫变化较大鼠更明显。
五、条件反射对免疫功能的影响(一)免疫性条件反射的研究概观 俄国学者的早期研究工作已发现可针对免疫应答建立起经典式条件反射。至70年代,采用以免疫抑制药物环磷酰胺为非条件性刺激(unconditionedstimulus, US),以饲饮糖精水的味觉刺激作为条件刺激(conditioned stimulus,CS),同时给大鼠上述两种刺激,经过一段时间后(3日),再单独给予CS,可引起明显的免疫抑制,表明为T细胞依赖性抗体(抗SRBC)合成减少,而对照组均无此反应,说明已建立起能改变免疫应答的行为式条件反射。以后的研究表明,同样可建立起对细胞免疫的条件反射,并可用以延长患自身免疫性疾病(红班狼疮)小鼠的寿命。另外,条件反射也可导致免疫增强效应,如提高NK细胞活性等。表10-4归纳了行为式条件反射引起的免疫应答改变。 表10-4 行为式条件反射引起的免疫效应变化
引自:Grossmann,Hervberman和Livnat(1992) (二)免疫性条件反射的发生机理假说 条件刺激引起免疫功能改变的机制尚不清楚,GC浓度上升并不能完全解释条件反射导致的免疫抑制效应,因为以US刺激海豹发GC分泌时并不改变免疫应答。目前有两种学说解释条件反射的免疫调节机理。 1.脑内关联性学习模式(associative brain learning paradigm) 该学说认为US引起的免疫信息和CS信息作为两个相关信号,可激活两种神经通路,并且在两个中枢神经环路间建立和强化相关的联系(结构的功能性的)。嗣后单独给予CS时,这两个环路均被激活,由此引发针对免疫系统的选择性信号,即对免疫应答产生调节作用,以图10-3表示如下。
图1-3 脑内关联性学习过程模式 根据Grossmann,Heberman和Livnat等(1992)修改 注:US:非条件刺激 CS:条件刺激 IR:免疫应答 2.免疫系统内部的关联性学习模式 (associative learning within the immunesystem) 其核心内容是将CS的关联性学习过程定位于免疫系统内部。当抗原或药物刺激淋巴细胞时,某些淋巴细胞对由此生成的辅助信号的敏感性增强,同时中枢神经系统对条件刺激发生反应,引起外周激素或递质的释放增多。这样,激活的淋巴细胞可同时对两套信号发生反应,并有定型化免疫应答的记忆功能。当单独用CS刺激,CS引起相应的神经源性输出信号,产生对这些免疫识记细胞的重复刺激信息,导致此类细胞激活,引发定型化免疫应答。如同时给予CS和US,则免疫应答较单独给予CS时更为明显。条件反射对免疫功能调节的实质是同时激活的淋巴细胞和辅助细胞获得对CS和US双重信号发生识记和定型反应的能力,以图10-4表示。 (三)免疫性条件反射发生途径实验分析 目前,许多证据支持前述第一假说,如以樟脑气味为CS,以Poly I-C为US,在小鼠建立起条件反射,结果引起脾脏中NK细胞活性增高。以后单用CS亦可观察到NK细胞的活性上升。进一步分析了这一条件反射的发生机制及途径,取得下述认识。 (1)由于Poly I-C能模拟病毒感染而明显促进IFN-β的分泌,因此单用IFN-β可取代Poly I-C成为US。
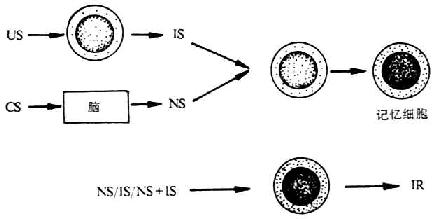
图10-4 免疫系统内的关联性学习模式 注:CS:条件刺激 US:非条件刺激 IS:免疫信号 NS:神经系号 IR:免反应答 (2)为探讨IFN-β是如何参与反射建立的,向枕大孔池注射100U的IFN-β也引起脾脏中NK细胞活性上升,而同剂量的IFN-β静注无效;将IFN-β抗体注入枕大孔池,可阻断条件反射的建立,但不影响US引起的反应。 (3)US以剂量依赖性方式影响免疫功能,如PolyI-C 10μg/小鼠能增加脾脏的NK细胞活性,但所生成的IFN-β少,不足以建立条件反应。PolyI-c 20μg/小鼠足以升高脾脏中IFN-β、IFN-α及其mRNA。以IFN-β注入体内作为US时,其剂量需达10000U方有效,而向枕大孔池中注入100U的IFN-β即可生效,因此以PolyI-C为US的中介信号为IFN-β,此信号可上传到脑内。 (4)CS为嗅觉刺激,US为给予免疫增强剂OolyI-C,此二种信号整合的部位可能在下丘脑。已发现条件反射的建立受多种因素的影响:预先给予纳屈酮阻断阿片肽的效应也阻断条件反应的出现,但用不透过血脑屏障的阿片受体阻断剂QNTX则无效,提示CS引起NK细胞活性上升的条件反射可能需阿片肽的参与,且可能作用于中枢神经部位。 (5)以药物耗竭中枢儿茶酚胺,可防止条件反应的发生,提示中枢内儿茶酚胺参与条件反射的建立和再现。 上述结果说明,条件反射的建立涉及两种记忆,其一为存贮于嗅觉系统中的CS记忆,其二为CS和US关联记忆,存贮于感觉系统以外的中枢部位,有可能是下丘脑。这与第一个学说相吻合。
…… 第三节 抗独特型抗体及其在医学研究中的应用 参考文献 第十章 神经免疫内分泌学引论 第一节 神经免疫内分泌学的发展简史 第二节 神经、免疫及内分泌系统间的关系 第三节 神经和内分泌(或神经内分泌)系统对免疫系统的调控(当前页) 第四节 免疫系统对神经内分泌系统的调控 第五节 神经免疫内分泌调节环路 参考文献 【完】 |