|
《医学遗传学基础》 > 第八章 药物遗传学
第一节 药物反应的遗传基础
一、琥珀酰胆碱敏感性琥珀酰胆碱(succinylcholine,suxamethonium)是一种肌肉松弛剂,早期作为外科麻醉剂使用,它不仅可使一般骨骼肌松弛,而且可使呼吸肌短暂麻痹(2-3分钟),但有极少数人(1/2000)在用药后呼吸停止可持续一小时以上,如不行人工呼吸,往往导致死亡。但若立即输血,呼吸可很快恢复。后来知道,琥珀酰胆碱在血中可被血浆中假胆碱酯酶(pseudocholinesterase,简称酯酶)水解而解毒,故作用短暂。琥珀酰胆碱敏感者,血浆酯酶活性缺乏或缺如,使琥珀酰胆碱作用时间延长,以致中毒。 现知琥珀酰胆碱敏感性是属常染色体隐性遗传,控制酯酶的基因为E1和E2。已发现的变异型有5种:E1a、E1a、Ef1、E1s、E+2及E2cynthiana。其中仅纯合子E1sE1s酯酶活性最低(酶活性0-5%),较常见的E1aE1a型酶活性也低35%。
二、异烟肼慢灭活异烟肼(isoniazid)是常用的抗结核药。在体内主要通过N-乙酰基转移酶(N-acetyltransferase,简称乙酰化酶)。将异烟肼转变为乙酰化异烟肼而灭活(图8-1)。按对异烟肼灭活的快慢,人群中可分出两类:一类称为快灭活者(rapid inactivator),血中异烟肼半减期为45-110分钟;另一类称为慢灭活者(slow inactivator),半减期2-4.5小时。而慢灭活者是由于乙酰化酶的遗传缺乏故灭活较慢。此酶系由常染色体一对等位基因控制。快灭活者(RR)与慢灭活者(rr)均为纯合子,杂合子(Rr)则具有中等乙酰化速度,不同种族慢灭活者发生率不同:埃及人高达83%,白种人50%左右,黄种人10%-30%,爱斯基摩人仅为5%。由于异烟肼乙酰化+速度的个体差异对结核病疗效有一定影响。如每周服药1-2次则快灭活者疗效较差。但从毒性作用看,慢灭活者有80%发生多发性神经炎(polyneuritis),而快灭活者仅20%有此副作用。这是由于异烟肼在体内可与维生素B6反应,使后者失活,从而导致B6缺乏性神经损害,故一般服异烟肼需同时服用B6可消除此种副作用。此外,服用异烟肼后有个别人可发生肝炎,甚至肝坏死。发生肝损害者中86%是快灭活者,其原因是,乙酰化异烟肼在肝中可水解为异烟酸和乙酰肼,后者对肝有毒性作用。
图8-1 异烟肼的灭活过程 通过N-乙酰基转移酶进行乙酰化灭活的药物尚有磺胺二甲嘧啶、苯乙肼、普鲁卡因酰胺、甲基硫氧嘧啶、肼苯达嗪、氨苯砜等。对这些药物快慢灭活的临床意义仅有一些零星材料,尚需进一步探讨。
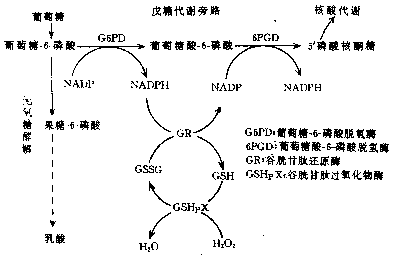
三、葡萄糖-6-磷酸脱氢酶缺乏症葡萄糖-6-磷酸脱氢酶(glucose-6-phosphate dehydrogenase,G6PD)缺乏症是一种主要表现为溶血性贫血的遗传病,一般平时无症状,但在吃蚕豆或伯氨喹啉类药物后出现血红蛋白尿、黄疸、贫血等急性溶血反应。 众所周知,红细胞中糖代谢主要是通过无氧糖酵解进行,但也有10%通过戊糖代谢旁路(图8-2)。G6PD活性正常是,可以生成足量NAKPH,从而保证了红细胞中GSH含量。GSH通过下列反应可消除机体在氧化还原过程中(特别是气体性药物作用下)生成的H2O2的毒性作用。
不难看出,若G6PD缺乏,NADPH生成不足,则红细胞GSH含量减少,H2O2可迅速将GSH破坏,过多的H2O2氧化Hbβ链表面半胱氨酸的SH基。表面SH氧化后,Hb的4条肽链接触面不稳定而散开,Hb内部的SH也被氧化,导致Hb变性。变性的珠蛋白附着于红细胞膜上,在显微镜下可观察到,即变性珠蛋白小体(Heinz小体)。此外,H2O2还可氧化红细胞膜上的SH基,故这种红细胞易在血中破坏。最近研究表明,NADPH的减少本身,也降低了红细胞对H2O2的抵抗作用。由于以上原因,红细胞变形性降低,不易通过脾(或肝)窦而遭阻留破坏,引起血管内和血管外溶血。
图8-2 红细胞的戊糖代谢旁路 基因突变所产生G6PD生化变异型已报告400种以上。中国人中已发现30多种。根据临床表现可分为二类:①酶活性严重缺乏(酶活性测不出)伴有非代偿性慢性溶血(属非球形溶血性贫血);②酶活性严重缺乏(活性<10%)或中度缺乏(10%-60%),仅在有诱因作用后才溶血,我国多为后一类。也有酶活性轻度降低、正常(60%-150%)或升高(>150%)的变异型,一般无溶血现象。
图8-3 G6PD缺乏症女性杂合子的外周血片示嵌合体,细箭头示正常红细胞;粗箭头示G6PD缺乏红细胞 G6PD基因定位于Xq28,由13个外显子组成,全长18kb,编码515个氨基酸。G6PD缺乏症呈X连锁不完全显性遗传,男性半合子呈显著缺乏,女性杂合子酶活性变异范围大,可接近正常亦可显著缺乏。根据Lyon假说,女性杂合子实际上应是含有G6PD缺乏红细胞和正常红细胞的嵌合体,这已从形态学上证实(图8-3),两种细胞系的细胞嵌合数量不同直接影响女性(G6PD)缺乏杂合子的酶活性水平,故在临床上具有不同的表现度。 由于生化变异型已报告太多,靠酸蛋白的生化学特点(如电泳速率,热稳定性等)来区分出新的变异型已很困难。自1986年克隆了此基因,特别是1991年发表了此基因的DNA全顺序后,就已从DNA水平鉴定G6PD基因的突变类型。目前已知,G6PD基因的主要突变形式是点突变。国际上报告了50多种点突变和1种1个密码子缺失的缺失型突变,其中中国人已报告11种点突变(表8-1)。不同生化变异型可以具有相同的点突变;也有不同点突变具有同一生化异型。有的突变只产生多态性而与酶活性降低无关。 表8-1 中国G6PD缺乏者中的11种点突变
注:Ch3的内含子Ⅺ93位有C→T突变。Ch3突变为为一种同义突变,具有多态特点 G6PD缺乏症呈世界性分布,但比较集中于亚热带地区。据估计全球G6PD缺乏症患者达2亿人。我国主要分布于黄河流域以南各省,尤以广东、广西、海南、贵州、云南、四川发生率高,约4%-20%。 G6PD缺乏症是某些常见药物性溶血的遗传基础。已知能引起G6PD缺乏者溶血的药物和化学制剂有数十种之多,有不少是常用药物(图8-2)。故G6PD缺乏症患者因治疗必须使用表8-2中某些药物时,应在医生严密监护下使用。G6PD缺乏症尚是蚕豆病、新生儿黄疸、某些感染性溶血(如病毒性肝炎、流感、大叶性肺炎、伤寒、腮腺炎等)发生的遗传背景,其中新生儿黄疸引起核黄疸可导致患儿智力低下,甚至死亡。 表8-2 G6PD缺乏者应禁用或慎用的药和、化学制剂及食物
四、血卟啉症药物反应也可以在遗传病的基础上发生。血卟啉症(porphyrias)的急性发作就是一个典型的例证。血卟啉症是一组涉及血红素合成有关酶遗传性缺陷的疾病,除其中有些类型表现为对光敏感皮肤出现红斑、水疱、溃疡、感染等症状外,其余常见类型主要表现为急性腹痛、便秘、呕吐、周围神经运动障碍(如肌无力、麻痹)以及精神症状(幻觉、精神错乱、焦虑等),尿中和粪中卟啉及卟啉前体物质增多。不同酶缺乏是形成各种类型的遗传基础。病人的缓解期可无症状,仅有尿和粪中卟啉类物质排泄增多。但多种药物,可诱导急性发作,如巴比妥、利眠宁、眠尔通、磺胺类药、苯妥英钠、灰黄霉素、雌激素等。药物诱发本病发作的机理未明。有人认为,这些药物可以加速δ氨基γ酮戊酸(ALA)合成酶的合成。ALA增多因而生成的胆色素原(尿和粪卟啉前体物)也增多。预防本病发作的有效方法就是避免使用上述药物及其他诱发因素(如饮酒、日晒等)。 其他具有遗传基础的药物反应及其表现列于8-3。 表8-3 其他具有遗传基础的药物反应
…… 第七章 基因定位 第一节 基因定位的方法 第二节 基因定位的应用 第三节 人类基因组计划 第八章 药物遗传学 第一节 药物反应的遗传基础(当前页) 第二节 毒物反应的遗传基础 第九章 肿瘤与遗传 第一节 肿瘤的染色体异常 第二节 肿瘤发病的遗传机理 …… |