|
《医用化学》 > 第十一章 链烃
第四节 炔烃炔烃是含有碳碳三键(-C≡C-)的链烃。
R-C≡CH或R`-C≡C-R”可代表它们的构造式,碳碳三键(-C≡C-)是炔烃的官能团。 炔烃也是不饱和烃,通式是CnH2n-2,与二烯烃或环烯烃相同。
一、炔烃的同分异构现象和命名法炔烃由于碳链构造和三键位置的不同,也具有同分异构现象。不过因为三键支链的位置的限制,其异构体的数目要比碳原子数相同的烯烃为少。例如,含有五个碳原子的炔烃,只有三种同分异构体:
炔烃的命名法和烯烃相似。例如:
二、炔烃的物理性质在正炔烃的同系列中,C2~C4的炔烃是气体,C5~C15的是液体,C15以上的是固体。炔烃的熔点和沸点也随着碳原子数目的增加而增高(表11-5)。 表11-5炔烃的物理常数
三、炔烃的化学性质炔烃的官能团是-C≡C-,它有两个π键,有较弱的亲核性(Lewis碱),其化学性质与烯烃有不少相似之处,例如能发生加成、氧化和聚和反应等。另外,-C≡C-H的C-Hσ键具有与 或 σ键不同的性质,即弱酸性很。 (一)加成反应 1.加氢 在催化剂(Pt,Pd或Ni)的作用下,炔烃与氢加成可生成烯烃,最后生成烷烃。
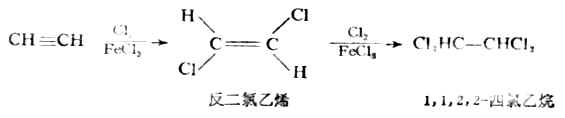
2.加卤素 炔烃能与氯或溴加成。反应分两步进行,第一次加1mol试剂,生成烯烃的二卤衍生物;第二次再加1mol试剂,生成四卤代烷。例如:
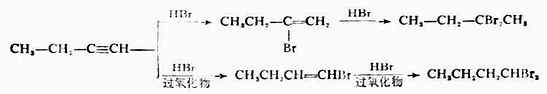
3.加卤化氢 炔烃和卤化氢的加成反应也是分两步进行的。
1,1-二溴乙烷 在生成的溴乙烯分子中,溴原子的未共用电子对与π键形成共轭体系(p-π共轭),这里共轭效应起了主要作用,而溴原子的诱导效应仅居次要地位。因此,当与第二个溴化氢分子加成时,溴原子继续加在已有一个溴的碳原子上,生成CH3CHBr2。 不对称炔烃与HX加成时遵从马氏规则。在有过氧化物存在下,不对称炔烃与HBr的加成反应则是反马氏规则的。 (二)氧化反应 炔烃氧化时,碳链在三键处断裂。例如,乙炔用高锰酸钾氧化时,生成二氧化碳。
其它炔烃用高锰酸钾氧化,生成羧酸。
从反应结果可以看到高锰酸钾的紫色消失,所以也可利用此反应检查碳碳三键。 (三)聚合反应 乙炔在不同的催化剂和反应条件下,发生各种不同的聚合反应,生成链状或环状的化合物。如乙炔若发生二分子聚合反应时,生成乙烯基乙炔CH2=CH-C≡CH;若在适当的催化剂存在下,三个分子的乙炔聚合成苯。
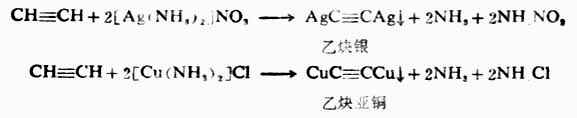
(四)炔化物的生成 连接在C≡C碳原子上的氢原子相当活泼,这是因为三键C是sp杂化,s成分占1/2,电负性比较强,使得Csp-H1sσ键的电子云更靠近碳原子,增强了C-H键极性,使氢原子容易离解,显示酸性。乙炔基阴离子能量低,体系稳定,所以乙炔分子CH≡CH中氢原子容易被金属取代,生成的炔烃金属衍生物叫做炔化物。例如,将乙炔通入硝酸银氨溶液或氯化亚铜氨溶液中,分别生成白色的乙炔银和砖红色的乙炔亚铜沉淀。
上述反应极为灵敏,常用来鉴定具有-C≡CH构造特征的炔烃,并可利用这一反应从混合物中把这种炔烃分离出来。而R`-C≡C-R型的炔烃不发生这两个反应。乙炔银和乙炔亚铜在湿润时比较稳定,在干燥时能因撞击或升高温度发生爆炸,所以实验完毕后,应立即加硝酸把它分解掉。
|